




Next: Wärmekapazitäten
Up: Thermodynamik
Previous: Thermodynamische Arbeit
Contents
Index
Subsections
Erster Hauptsatz - Energieerhaltung
Um die Energieerhaltung auch auf Thermodynamische Systeme auszudehnen,
muss man ihnen eine Energie zuordnen. Dies ist die Wärme. Sie besteht
aus den mikroskopischen kinetischen Energien der einzelnen Teilchen
im System.
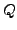 ist extensive Größe
ist extensive Größe 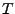 aber nicht. Also ist auch
aber nicht. Also ist auch 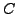 eine
extensive Größe.
eine
extensive Größe.
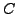 bezeichnet die Wärmekapazität eines Systems
bezeichnet die Wärmekapazität eines Systems
- Man kann ein
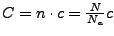 definieren
definieren
Für die innere Energie 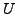 gilt
gilt
Mit Austasch von Teilchen gilt allgemeiner
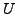 ist eine Zustandsgröße, es gilt also
ist eine Zustandsgröße, es gilt also
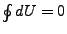
- In einem isolierten System (kein Wärmeaustausch mit der Umgebung)
ist
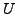 daher eine Erhaltungsgröße und es gilt
daher eine Erhaltungsgröße und es gilt
kalorische Zustandsgleichung
Bei einem idealen Gas gilt
mit 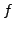 der Anzahl der Freiheitsgerade des Gases.
der Anzahl der Freiheitsgerade des Gases.





Next: Wärmekapazitäten
Up: Thermodynamik
Previous: Thermodynamische Arbeit
Contents
Index
Marco Möller 17:08:30 24.10.2005
![]() gilt
gilt
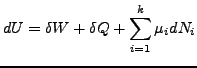
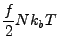
![]() der Anzahl der Freiheitsgerade des Gases.
der Anzahl der Freiheitsgerade des Gases.