




Next: 2. HS der Wärmelehre
Up: Reale Gase
Previous: Zustandsgleichung
Contents
Index
- Dampfdurckkurve
- Geht vom Trippelpunkt bis zum Kritischen Punkt.
Flüsssige und gasförmige Phase existieren gleichzeitig. Oberhalb flüssig,
unterhalb Gasförmig
- Schmelzkurve
- Beginnt im Trippelpunkt, hat aber nach oben hin kein
Ende. Feste und flüssige Phase existieren gleichzeitig. Links Fest,
rechts flüssig.
- Sublimationskurve
- feste und Gasförmige Phasen existieren gleichzeitig.
Endet im Tripelpuntk und beginnt in der Nähe des Ursprungs. Oben fest,
Rechts flüssig
- Dampfdruck
- Druck des Gases, der sich im Raum über einer Flüssigkeit
einstellt. Ebensoviele Molekühle verlassen die Flüssigkeit wie in
Sie zurückkehren.
- Latente Wärme
- (gespeicherte Wärme) Übergang einer Stoffmenge von
der Phase
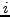 in die Phase
in die Phase 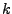 .
.
Wärmemenge
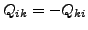 . Ist
. Ist 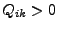 muss sie dem System
zugeführt werden, für
muss sie dem System
zugeführt werden, für 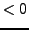 gibt das System sie ab.
gibt das System sie ab.
- spezifische Phasenübergangswärme
-
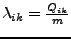
-
![$ \left[\lambda\right]=\frac{Ws}{kg}$](img222.png)
- spez. Schmelzwärme
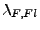
- spez. Verdampfungswärme
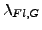
- spez. Sublimationswärme
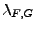
- Phasenübergang 1. Ordnung
- heißen Phasenübergange, bei denen sich
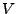 (bei
(bei 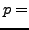 konst) und
konst) und 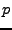 (bei
(bei 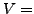 konst) eines Systems bei
einer Übergangstemperatur
konst) eines Systems bei
einer Übergangstemperatur
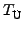 ändert. D.h.
ändert. D.h.
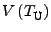 und
und
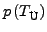 verhalten sich unstetig.
verhalten sich unstetig.
- Phasenübergang 2. Ordnung
- heißen Phasenübergange, bei denen sich
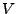 und
und 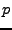 stetig an
stetig an
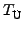 verhalten, aber
verhalten, aber
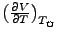 und
und
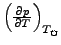 unstetig verhalten. Hier gibt es also keine Änderung der potentiellen
Energie des Systems, d.h. es gibt keine latenten Wärmen. Phasenumwandlungen
erfolgen also ohne Energiezufuhr,
unstetig verhalten. Hier gibt es also keine Änderung der potentiellen
Energie des Systems, d.h. es gibt keine latenten Wärmen. Phasenumwandlungen
erfolgen also ohne Energiezufuhr, 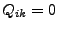
-
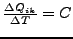 ist also abgeknickt beim Übergang.
ist also abgeknickt beim Übergang.





Next: 2. HS der Wärmelehre
Up: Reale Gase
Previous: Zustandsgleichung
Contents
Index
Marco Möller 16:43:44 24.10.2005